
Инфекции верхнего респираторного тракта, такие как острый фарингит, – наиболее распространенное заболевание, встречающееся в практике врача–интерниста. От 40% до 60% всех случаев острого фарингита вызваны вирусной инфекцией, 5–40% – бактериальной флорой. Среди многообразия вирусных агентов (вирусы гриппа, парагриппа, риновирус, аденовирус, респираторно–синтициальный вирус, коронавирус), вызывающих острые респираторные заболевания, риновирус и коронавирус чаще всего приводят к развитию фарингита.
Различные серотипы (А, B, C, G, F) группы бета–гемолитического стрептококка (БГС) вида Str. pyogenes являются наиболее частыми возбудителями острого бактериального фарингита, среди которых на долю БГС–А приходится 15–17% случаев у взрослых и до 30% – у детей. БГС серотипов B, C, G, F составляют около 10% случаев стрептококковых фарингитов. Ежегодно в России регистрируется 6–8 млн случаев респираторной стрептококковой инфекции. По выражению Rotta, «пока существует человек, избавиться от стрептококка нельзя, т.к. именно человек является резервуаром для стрептококка». Острые фарингиты, ассоциированные с Arcanobacterium haemolyticum, Neisseria gonorrhoeae, Corynebacterium diphteriae, встречаются редко. Mycoplasma pneumonia и Сhlamidia pneumonia, наряду с поражением нижних дыхательных путей, могут вызывать развитие острого фарингита.
Помимо острого фарингита БГСА ответственен за возникновение ряда заболеваний, имеющих различные варианты развития и исходы, что подтверждает актуальность и мультидисциплинарность стрептококковых заболеваний (табл. 1).
В ряде случаев стрептококковая инфекция глотки может прогрессировать и вызывать абсцессы в ткани миндалин, перитонзиллярных или ретрофарингеальных тканях, шейный лимфаденит, синусит, средний отит, мастоидит и даже менингит. Значительный процент фарингеальных инфекций, подтвержденных значительным повышением титра антистрептококковых антител, характеризуется весьма умеренной клинической симптоматикой или даже бессимптомным течением. Тем не менее, они ассоциируются с риском поздних осложнений и в отличие от «хронических носителей» могут быть активным источником распространения вирулентного стрептококка.
Из первичных кожных инфекций, вызванных БГСА, чаще всего встречается импетиго (пиодермия), особенно в условиях тропического климата. Другие проявления включают рожистое воспаление, локальные нагноения в результате микротравм и ран, гнойные поражения подкожной клетчатки (в том числе перианальной области). С кожной инфекцией связывают некоторые редкие, но тяжелые случаи некротизирующего фасциита и миозита.
Третья группа первичных стрептококковых инфекций – гинекологические заболевания: вульвовагиниты и послеродовый сепсис, которые хотя и нечасто, но встречаются во многих странах.
Инфекционные поражения глотки, кожи и гениталий могут осложняться угрожающими жизни состояниями, такими как септикопиемия, инфекционно–токсический шок, развитием метастатических гнойных очагов: артрита, остеомиелита, перитонита и даже острого эндокардита. БГСА уникален по своей способности вызывать поздние негнойные осложнения, например гломерунонефрит, который может развиться после инфицирования как глотки, так и кожи нефротропными штаммами, и ревматическую лихорадку, которая развивается только после инфицирования глотки.
Во многих развивающихся странах большой социальной проблемой является ревматическая болезнь сердца. Кроме того, имеются данные о спорадических вспышках ревмокардита, что служит напоминанием о сохраняющейся актуальности этой проблемы. Этиологическая связь между инфекцией, вызванной БГСА, и последующим развитием РЛ хорошо известна.
Ревматическая лихорадка (РЛ) – это постинфекционное осложнение А–стрептококкового тонзиллита/фарингита у предрасположенных лиц с развитием аутоиммунного ответа на эпитопы стрептококка группы А и перекрестной реактивности со сходными эпитопами тканей человека (сердце, суставы, ЦНС). В развитых странах уровень заболеваемости РЛ понизился со 100–250 до 0,23–1,88 на 100 тыс. населения. Тем не менее, в мире на настоящий момент страдают РЛ и ревматической болезнью сердца (РБС) около 12 млн человек.
РЛ протекает в виде атак. У 70% больных ревматическая атака стихает по клинико–лабораторным данным в течение 8–12 нед., у 90– 95% – в течение 12–16 нед., и лишь у 5% больных атака продолжается более 6 мес., т.е. принимает затяжное либо хроническое течение.
Кардит, артрит, хорея, кольцевидная эритема и подкожные узелки являются большими диагностическими признаками ОРЛ.
Кардит является наиболее важным признаком РЛ, определяющим тяжесть состояния больного и болезни. Кардит может возникать изолированно или сочетаться с другими основными клиническими проявлениями РЛ. Воспалительные и дистрофические изменения в сердце при РЛ могут поражать все его слои с развитием эндокардита (вальвулита), миокардита, перикардита. По частоте поражения при РЛ лидирует митральный клапан, далее по мере убывания следуют аортальный, трикуспидальный и клапан легочной артерии.
В настоящее время выделяют международные клинические критерии кардита:
• органический шум (шумы), ранее не выслушиваемый, или динамика ранее существовавших шумов,
• увеличение сердца (кардиомегалия),
• застойная сердечная недостаточность у молодых лиц,
• шум трения перикарда или признаки выпота в полость перикарда.
К шумам, свидетельствующим о наличии кардита, эксперты ВОЗ относят:
• интенсивный систолический шум над верхушкой,
• мезодиастолический шум над верхушкой (шум Carey Coombs),
• базальный протодиастолический шум.
Легкий кардит диагностируется при появлении шумов в сердце без изменения его размеров и функции. Среднетяжелый кардит определяется при выявлении шумов в сердце в сочетании с увеличением его размеров, а тяжелый – при определении шумов в сердце в сочетании с кардиомегалией и застойной сердечной недостаточностью и/или перикардитом.
Ревматический порок сердца формируется как исход ревмокардита. Максимальная частота развития пороков сердца наблюдается в первые 3 года от начала заболевания. Наиболее часто развиваются стеноз левого атриовентрикулярного отверстия, митральная регургитация, недостаточность аортального клапана и аортальный стеноз, а также сочетанные и комбинированные пороки сердца.
Ревматический артрит. Артрит – наиболее частое проявление РЛ, присутствующее у 75% пациентов при первой атаке. Суставные проявления при РЛ могут варьировать от артралгии до артрита, протекающего с болевой контрактурой. В классическом нелеченном случае артрит поражает несколько суставов быстро и последовательно, каждый на короткое время, поэтому для описания полиартрита при ОРЛ широко используется термин «мигрирующий». Наиболее часто поражаются крупные суставы нижних конечностей (коленные и голеностопные), реже – локтевые, лучезапястные, плечевые и тазобедренные, а мелкие суставы кистей рук, стоп и шеи вовлекаются совсем редко. В типичном случае каждый сустав остается воспаленным не более одной–двух недель, а полностью артрит разрешается в течение месяца, даже при отсутствии лечения. Естественное течение полиартрита при ОРЛ изменяется при использовании в рутинной практике салицилатов и других нестероидных противовоспалительных препаратов (НПВП).
Ревматическая хорея. Ревматическая хорея (Sydenham’s хорея, малая хорея или «пляска святого Вита») характеризуется эмоциональной лабильностью, некоординированными движениями и мышечной слабостью. Хорея главным образом встречается у детей, после 20 лет наблюдается редко. Как правило, она развивается у девочек и почти никогда у мальчиков в постпубертатном периоде. Распространенность хореи у пациентов с РЛ варьирует от 5% до 36%. Хорея как один из критериев РЛ имеет ряд особенностей: более длительный латентный период после стрептококковой инфекции, составляющий 1–7 мес., в результате чего полиартрит и Sydenham’s хорея практически не встречаются вместе; титры стрептококковых антител, лабораторные признаки воспаления стихают к моменту появления хорееформных движений. В 1/3 случаев отмечаются рецидивы хореи.
Подкожные узелки и кольцевидная эритема. Подкожные узелки и кольцевидная эритема – редкие проявления РЛ, они встречаются менее чем в 10% случаев.
Подкожные узелки – это круглые, плотные, легко смещаемые, безболезненные образования размером от 0,5 до 2 см, чаще локализующиеся на разгибательных поверхностях локтевых, коленных и других суставов, в затылочной области и по ходу сухожильных влагалищ, крайне редко бывают при первой атаке РЛ. Число узелков варьирует от одного до нескольких десятков, но обычно их 3–4. Считается, что их легче прощупать, чем увидеть. Они сохраняются от нескольких дней до 1–2 недель, реже – больше месяца. Подкожные узелки почти всегда ассоциируются с вовлечением сердца и обнаруживаются чаще у пациентов с тяжелым кардитом.
Эритема – это преходящие кольцевидные пятна с бледным центром, как правило, возникают на туловище, шее, проксимальных отделах конечностей. Кольцевидная эритема никогда не локализуется на лице. В связи с мимолетностью изменений и отсутствием ассоциированных симптомов кольцевидная эритема может быть пропущена, если ее специально не искать, особенно у темнокожих пациентов. Кольцевидная эритема обычно появляется в начале ревматической атаки. Однако она может персистировать или рецидивировать в течение месяцев или даже лет, сохраняясь после того, как другие проявления заболевания стихнут, и на них не влияет противовоспалительная терапия. Этот кожный феномен ассоциируется с кардитом, но, в отличие от подкожных узелков, не обязательно с тяжелым. Узелки и кольцевидная эритема часто сочетаются.
Артралгии и лихорадку обозначают как «малые» клинические проявления РЛ в диагностических критериях Т. Джонса не потому, что они встречаются реже, чем пять больших критериев, а потому, что обладают меньшей диагностической специфичностью. Лихорадка наблюдается в начале почти всех ревматических атак и обычно составляет 38,4–40oС. Обычно отмечаются колебания в течение дня, но характерной температурной кривой нет.
В настоящее время в соответствии с рекомендациями ВОЗ в качестве международных применяются диагностические критерии РЛ Т. Джонса, пересмотренные в 2002 г. (табл. 2).
Для подтверждения первичной атаки заболевания должны иметься большие и малые критерии РЛ, лабораторные изменения и доказательства предшествующей стрептококковой инфекции в соответствии с рекомендациями ВОЗ 2004 г. В контексте перенесенной стрептококковой инфекции два больших критерия или комбинация одного большого и двух малых являются достаточным основанием для диагностики ОРЛ. Диагноз повторной РЛ у пациента с установленной РБС может ставиться на основании малых критериев в сочетании с доказательством недавно перенесенной стрептококковой инфекции (табл. 3).
Свидетельством недавно перенесенной стрептококковой инфекции является повышение титров стрептококковых антител, определяемых в парных сыворотках (табл. 4), которое наблюдается в течение первого месяца от начала заболевания, сохраняется, как правило, в течение 3 мес., нормализуясь через 4–6 мес.
Особого внимания, с клинической точки зрения, заслуживает «постстрептококковый артрит», описанный Friedberg С. в 1959 г. как артрит, развившийся у взрослых после ангины, без явлений кардита и ассоциирующийся с повышенными титрами антистрептолизина–О (АСЛ–О) в сыворотке крови. В начале 1980–х гг. Goldsmith D. и Long S. описали наблюдение 12 детей с длительно текущим артритом, развившимся в короткий срок после стрептококковой инфекции. Клиническая картина заболевания не укладывалась в классические рамки критериев ревматической лихорадки (РЛ). Артрит у них протекал длительно – от нескольких недель до нескольких месяцев и был слабо чувствителен к терапии салицилатами и другими НПВП. Течение болезни больше напоминало течение реактивного артрита, а признаков поражения сердца найдено не было.
Таким образом, отличительными особенностями постстрептококкового артрита являются [Deighton C., 1993]: короткий латентный период между острой стрептококковой инфекцией и манифестацией заболевания (1–2 нед.), недостаточный эффект НПВП и длительное течение артрита, отсутствие кардита и серьезность артрита, наличие экстраартикулярных поражений (тендинит и др.).
Учитывая, хотя бы и редкую, возможность развития пороков сердца, неотличимых от ревматических, у пациентов с ПСА, для стандартизации подхода к проведению антибиотикопрофилактики Комитет экспертов ВОЗ в 1995 г. рекомендовал рассматривать ПСА в рамках РЛ, при этом не отвергая возможности применения самого термина «постстрептококковый артрит». Данному решению способствовало в том числе и то обстоятельство, что большинство пациентов, у которых обсуждался диагноз ПСА, соответствовали также и критериям Джонса для постановки диагноза РЛ. Тем не менее, нозологическая принадлежность ПСА до сих пор является неопределенной, а данная тема остается в центре внимания клиницистов многих стран, т.к. обоснование рекомендаций ВОЗ по проблеме ПСА на фактическом материале является явно недостаточным.
Учитывая широкий спектр вторичных форм стрептококковой инфекции, представляется важным своевременный подход к диагностике и антибактериальному лечению первичных форм заболевания, в том числе острого фарингита.
К наиболее типичным клиническим проявлениям острого фарингита относят боль в горле при глотании («пустой глоток»), гиперемию зева и миндалин с/без экссудата, петехии мягкого и твердого неба. Бактериологическое исследование мазка из зева является «золотым стандартом» диагностики БГС, однако он не может использоваться в повседневной рутинной практике, кроме того, он не позволяет дифференцировать активную инфекцию и стрептококковое носительство.
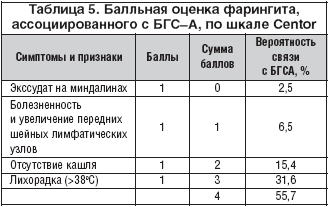
За истекшие 40 лет предпринимались различные попытки совершенствования клинической физикальной диагностики стрептококковых и вирусных фарингитов. Наиболее информативной и доступной в использовании является шкала Centor, рекомендованная к практическому применению American College of Physicians American Society of Internal Medicine (ACP/ASIM) and Centers for Disease Control and Prevention (CDC) в США. Она включает сочетание 4 симптомов и признаков, позволяющих на этапе физикального осмотра провести дифференциальный диагноз между вирусным и бактериальным фарингитом, вызванным бета–гемолитическим стрептококком (табл. 5). ACP/ASIM рекомендуют проводить антибактериальную терапию пациентам с тремя критериями из четырех, а также в сомнительных случаях при обнаружении 2–3 критериев проводить быстрый тест обнаружения антигена (RADT–тест) и не применять антибиотики во всех других случаях. National Institute for Health and Clinical Excellence (NICE) в Великобритании рекомендует использовать в лечении острого фарингита антибактериальные препараты при наличии трех и более критериев шкалы Centor. Модифицированная версия критериев Centor также рекомендована к применению в Новой Зеландии.
Алгоритм ведения пациентов с острым фарингитом согласно оценочной шкале Centor, разработанный на кафедре факультетской терапии им. академика А.И. Нестерова РНИМУ, представлен в таблице 6.
Лечение острого вирусного фарингита направлено на облегчение симптомов заболевания. Традиционно для лечения острых фарингитов используют полоскания щелочными и дезинфицирующими растворами, обильное теплое питье. В лечении острого фарингита, ассоциированного с БГСА, придерживаются следующих направлений:
• симптоматическая терапия;
• антибактериальная терапия (первичная профилактика РЛ);
• профилактика септическо–токсических осложнений.
В качестве антибактериальных препаратов используются антибиотики пенициллинового ряда в течение 10 дней (пенициллин V (феноксиметилпенициллин) детям: 250 мг 2–3 раза/сут. (≤27 кг), детям >27 кг, подросткам и взрослым – 500 мг 2–3 раза/сут., амоксициллин 60 мг/кг 1 раз/сут., макс. 1000 мг, бензатинпенициллин G 600 тыс. ЕД (≤27 кг), 1 млн 200 тыс. ЕД (>27 кг) внутримышечно однократно. При аллергии к пенициллинам используются макролиды клиндамицин 20 мг/кг/сут. в 3 приема (макс. 1,8 г в сутки), кларитромицин 15 мг/кг/сут. в 2 приема (макс. 250 мг 2 раза/сут.) – 10 дней, азитромицин 12 мг/кг 1 раз/сут. (макс. 500 мг) – 5 дней.
В качестве симптоматической терапии рекомендуется использовать системные и локальные противовоспалительные средства лечения. Одним из современных НПВП является препарат ОКИ (Dompé laboratory, Италия). Он представляет собой соединение кетопрофена с аминокислотой лизин, позволяющее достигнуть значительного улучшения фармакокинетических свойств действующего вещества по сравнению с обычным кетопрофеном. Это выражается в увеличении растворимости лекарства, биодоступности для тканей (высокая концентрация в тканях миндалин), более быстром всасывании и раннем развитии терапевтического эффекта с пиком концентрации через 15 мин. (через 60 мин. у обычного кетопрофена).
ОКИ имеет нейтральный рН, в связи с чем риск гастропатии снижен (переносимость в 1,6 раза лучше в сравнении с обычным кетопрофеном). ОКИ выпускается в форме саше, ректальных суппозиториев и раствора для полоскания. Имеет улучшенный профиль эффективности противовоспалительной терапии фарингита и ларинготрахеита в форме саше по данным двойного слепого плацебо–контролируемого исследования в сравнении с нимесулидом саше, выражающийся в уменьшении таких показателей воспаления, как отек, боль, гиперемия (95% vs 86%).
Жаропонижающий эффект ОКИ – более выраженный, чем у других НПВП (ибупрофен, напроксен, фенопрофен). ОКИ оказывает более выраженный анальгетический эффект, чем парацетамол, у детей и является хорошей альтернативой для уменьшения боли (рис. 1).
ОКИ – единственный препарат из системных форм кетопрофенов, разрешенный к применению в педиатрии. ОКИ в форме ректальных суппозиториев у детей обеспечивает более выраженный эффект, чем у парацетамола в соответствующих возрастных дозировках (5 мг/кг веса в сутки, детская дозировка суппозиториев ОКИ–60 мг) (табл. 7).
В случаях установления РЛ назначается лечение пенициллином, обеспечивающим удаление БГСА из носоглотки. Из пенициллинов наиболее часто используют бензилпенициллин или феноксиметилпенициллин. Рекомендованные суточные дозы бензилпенициллина: детям – 400–600 тыс. ЕД, взрослым – 1,5–4 млн ЕД внутримышечно – по 4 введения в течение 10 дней. Феноксиметилпенициллин рекомендуется взрослым по 500 мг внутрь 2 раза/сут. в течение 10 дней. Пенициллины должны всегда рассматриваться как препараты выбора в лечении ОРЛ, за исключением случаев их индивидуальной непереносимости, когда назначают макролиды или линкозамиды. Симптоматическая терапия ревмокардита проводится НПВП и глюкокортикостероидами. Лечение повторных атак РЛ не отличается от ведения больных с первичной атакой.
Профилактика рецидива РЛ должна назначаться сразу в стационаре после окончания 10–дневного лечения пенициллинами (макролидами, линкозамидами). Классический парентеральный режим – это бензатинпенициллин G 1,2–2,4 млн ЕД в/м 1 раз/3–4 нед. При аллергии на пенициллины могут быть использованы макролиды на выбор из схемы первичной профилактики РЛ.







Литература
1. Шостак Н.А., Карпова Н.Ю., Абельдяев Д.В. и соавт. Постстрептококковый артрит. // Научно–практическая ревматология, 2003, 4:77–82 .
2. Acerra J. R., Andrew Aronson. Pharyngitis. eMedicine. Eds. Jerry Balantine, et al. 5 Nov. 2007. Medscape. 26 Jun. 2009
3. Halsey Eric. Pharyngitis, Bacterial. eMedicine. Eds. Klaus–Dieter Lessnau et al. 19 May. 2009. Medscape. 26 Jun. 2009 http://emedicine.medscape.com/article/225243–overview
4. Mirza A., Wludyka P., Chiu T.T., Rathore M.H. Throat cultureis necessary after negative rapid antigen detection tests. // Clin Pediatr (Phila) 2007, 46:241–246.
5. Anonymous: Diagnosis and treatment of streptococcal sore throat. Drug Ther Bull 1995, 33 :9–12.
6. Centor R.M., Witherspoon J.M., Dalton H.P., Brody C.E., Link K.: The diagnosis of strep throat in adults in the emergency room. Med Decis Making 1981,1:239–246.
7. Jolien Aalbers, Kirsty KO Brien1, Wai Sun Chan et al. Predicting streptococcal pharyngitis in adults in primary care: asystematic review of the diagnostic accuracy of symptoms and signs and validation of the Centor score. BMC Medicine 2011, 9:67 http://www.biomedcentral.com/ 1741–7015/9/67
8. NICE Short Clinical Guidelines Technical Team: Respiratory tract infections–antibiotic prescribing. Prescribing of antibiotics for self–limiting respiratory tract infections in adults and children in primary care NICE clinical guideline 69. London: National Institute for Health and Clinical Excellence. 2008 [http://www.nice.org.uk/nicemedia/pdf/CG69FullGuideline.pdf].
9. Snow V., Mottur–Pilson C., Cooper R.J. , Hoffman J.R. Principles of appropriate antibiotic use for acute pharyngitis in adults. Ann Intern Med 2001, 134:506–508.
10. Kerdemelidis M., Lennon D., Arroll B., Peat B. Guidelines for sore throat managementin New Zealand. NZ Med J 2009,122:10–18.
11. M. A. Gerber, R. S. Baltimore, C. B. Eaton et al. Prevention of Rheumatic Fever and Diagnosis and Treatment of Acute Streptococcal Pharyngitis. Circulation 2009, 119:1541–1551.
12. de Lorenzi C. et al. Evaluation of therapeutic successes of ketoprofen lysine salt granular formulation (sachets) in patients with inflammatory disease of upper respiratory airways. Double–blind, double–dummy, controlled study versus Nimesulide granular formulation (sachets). Data on file 1997.
13. Bellussi L. et al. Antiphlogistic therapy with ketoprofen lysine salt vs nimesulide in secretory otitis media, rhinitis/rhinosinusitis, pharyngitis/tonsillitis/tracheitis. Note di Terapia Otorinolaringol, 1996; 46: 49–57.
14. Messeri A. et al. Analgesic efficacy and tolerability of Ketoprofen lysine salt vs paracetamol in common paediatric surgery. A randomized, single–blind, parallel, multicentre trial. Pediatric. Anesthesia 2003; 13: 574–8.
Шостак Н.А., Правдюк Н.Г., Аксенова А.В., Абельдяев Д.В.
РМЖ

 Опубликовано в категории:
Опубликовано в категории:  Метки:
Метки: