
Проблема лечения острого и хронического риносинуситов остается актуальной в современных условиях, так как ежегодно число пациентов с этой патологией увеличивается. В мире около 15% населения страдают риносинуситом. С учетом обращаемости в России более 10 млн. человек каждый год переносят различные формы риносинусита. Риносинуситы входят в десятку наиболее распространенных диагнозов в амбулаторной практике. По мнению ряда авторов, в структуре заболеваний в ЛОР–стационарах синусит составляет от 15 до 36%.
Рецидивы после хирургического лечения хронического синусита, по данным различных авторов, составляют от 20 до 60%. Основной процент рецидивов приходится на продуктивные (полипозные и полипозно–гнойные) формы хронического синусита.
К сожалению, хирургическое лечение полипозного синусита и послеоперационное ведение пациентов с данной патологией проводятся по одной схеме. Хотя по данным многочисленных научных исследований, по накопленному клиническому опыту доказано, что причины возникновения полипозного процесса в околоносовых пазухах (ОНП) различны. В этой связи и тактика лечения полипозного синусита должна носить дифференцированный подход, что позволит снизить процент рецидивов полипозного процесса.
Морфология и патогенез
Носовой полип состоит из поврежденного, иногда метаплазированного эпителия, расположенного на утолщенной базальной мембране, и отечной стромы, содержащей небольшое количество желез и сосудов и практически лишенной нервных окончаний. Строма типичного полипа содержит фибробласты, формирующие опорный каркас, псевдокисты и клеточные элементы, основными из которых являются эозинофилы, расположенные вокруг сосудов, желез и непосредственно под покровным эпителием.
Эозинофилы играют ключевую роль в патогенезе полипозного синусита, но пока неизвестно, каким именно образом эозинофильное воспаление приводит к образованию и росту полипов. Предполагают, что процесс рекрутирования эозинофилов может регулироваться цитокинами. Продуцируемые Th2–лимфоцитами цитокины (в частности, интерлейкин–3 и интерлейкин–5) могут вызывать эозинофилию, стимулируя пролиферацию эозинофилов в костном мозге и их выход в кровеносное русло, а также ингибируя их апоптоз (запрограммированную смерть). Недавние исследования дают основания предполагать, что интерлейкин–5 является ключевым фактором в патогенезе полипозного синусита, индуцирующим процессы хоуминга эозинофилов, их миграции в ткани и дегрануляции [1]. Одна из гипотез предполагает, что активированные эозинофилы мигрируют в слизистую оболочку, чтобы уничтожать грибки, которые попадают в полость околоносовых пазух при нормальном воздухообмене [2].
В результате дегрануляции эозинофилов в просвете околоносовых пазух образуется очень густой муцин, содержащий большое количество токсичных белков. В частности, главный протеин оказывает повреждающее действие на слизистую оболочку, вызывая в ней хронический воспалительный процесс и рост полипов. Выделяемые из гранул эозинофилов токсичные белки могут воздействовать и на электролитный обмен эпителиальных клеток, блокируя натриевые насосы и усиливая выход ионов хлора из клетки. В результате развивается интерстициальный отек, который также способствует росту полипов.
Еще один патогенетический механизм полипозного синусита, интенсивно изучаемый в последние годы – нарушение метаболизма арахидоновой кислоты и непереносимость нестероидных противовоспалительных препаратов. У больных полипозным синуситом происходит ингибирование фермента циклооксигеназы, что ведет к активизации альтернативного пути метаболизма арахидоновой кислоты, катализируемого 5 липоксигеназой.
Диагностика
Диагностика полипозного синусита складывается из комплексной оценки жалоб пациента, анализа данных анамнеза (аллергия, наличие симптомов бронхиальной астмы и т.д.), результатов инструментальных методов исследования. Основными методами инструментальной диагностики полипозного синусита являются: эндоскопия полости носа и носоглотки и компьютерная томография (КТ) ОНП.
Эндоскопия полости носа и носоглотки. Исследование выполняется после анемизации и однократного смазывания слизистой оболочки полости носа 10% раствором лидокаина эндоскопом диаметром 2,7 мм, 4 мм с торцевой и угловой оптикой 0°, 30°, 70°. Стандартное исследование включало в себя три основных этапа. Сначала эндоскоп проводится по нижнему носовому ходу, при этом оценивается цвет слизистой оболочки нижней носовой раковины, наличие и характер выделений на дне полости носа. Затем, по мере продвижения эндоскопа в носоглотку, определяются размеры задних концов нижних носовых раковин, а также состояние глоточной миндалины и устьев слуховых труб.
Второй этап исследования – проведение эндоскопа по среднему носовому ходу. При этом эндоскоп сначала ориентирован сагиттально, с осмотром переднего конца средней носовой раковины и крючковидного отростка. Затем дистальный конец эндоскопа продвигается между указанными образованиями, разворачивается в краниальном и латеральном направлениях и проводится оценка области воронки и решетчатой буллы.
Третий этап – введение эндоскопа в верхний носовой ход, идентификация верхней носовой раковины и, при возможности, естественных отверстий клиновидной пазухи и задних клеток решетчатого лабиринта.
КТ ОНП, выполненная в коронарной и аксиальной проекциях, является идеальным методом диагностики распространенности патологического процесса в ОНП. Также КТ способствует выявлению причин, приводящих к рецидиву синусита, уточнению индивидуальных особенностей строения полости носа и ОНП, способных стать причиной интраоперационных осложнений.
Дополнительными диагностическими мероприятиями у пациентов с полипозным синуситом нередко являются аллергодиагностика (цитологическое исследование мазков–отпечатков со слизистой оболочки полости носа (эозинофилия), определение общего и специфического Ig Е), определение функций внешнего дыхания с бронхолитиком, консультация пульмонолога и аллерголога, так как аллергический ринит и бронхиальная астма – частые «спутники» полипозного синусита.
Лечение
Поставив диагноз полипозный синусит, оториноларинголог, сопоставив данные жалоб, анамнеза, инструментальных методов исследования, должен определить вероятные причины развития полипозного процесса, так как от этого напрямую зависит результат лечения. При небольших полипах следует начать лечение с консервативной терапии, так как современный арсенал лекарственных препаратов при правильном использовании, индивидуальном подходе во многих случаях позволит избежать хирургического лечения. А ведь, как говорится: «Лучшая операция – это не сделанная операция». Другая ситуация при обтурирующем полипозе, когда есть все показания для хирургического лечения.
С практических позиций следует различать следующие группы полипозного процесса:
А. Полипоз, возникающий в результате нарушения аэродинамики полости носа, обусловленной особенностям архитектоники полости носа.
Б. Полипоз, развивающийся в результате хронического гнойного (бактериального) или грибкового воспаления околоносовых пазух.
В. Полипоз, развивающийся на фоне аспириновой триады (ассоциированный с атопической бронхиальной астмой, атопией).
Полипоз, возникающий в результате нарушения аэродинамики полости носа, обусловленной особенностям архитектоники полости носа
При искривлении перегородки носа, прежде всего при наличии локальных гребней в костном отделе, при вдохе (человек вдыхает в сутки более 20 000 раз) воздушная струя, отражаясь от гребня, ударяет в латеральную стенку носа в область остеомеатального комплекса. При этом происходит чрезмерное раздражение слизистой оболочки носа и ОНП, нарушение нормальной дренажной функции естественного соустья, аэрации синусов, а также формирование полипов.
Хирургическое лечение такой категории пациентов состоит в коррекции перегородки носа (септопластика, подслизистая кристотомия), полипэтмоидотомии, а также в операциях на нижних и средних носовых раковинах (вазотомия, нижняя щадящая конхотомия, порциальная резекция средней носовой раковины). Проведение медикаментозной терапии, направленной на профилактику возникновения рецидивов полипозного процесса, у пациентов данной группы не требуется.
Полипоз, развивающийся в результате
хронического гнойного (бактериального) или грибкового воспаления околоносовых пазух
Полипозный процесс в полости носа у пациентов данной группы развивается в результате длительного раздражения слизистой оболочки носа гнойным отделяемым воспаленных ОНП.
В настоящее время принято считать, что при хроническом синусите бактериальный спектр чаще представлен микробными ассоциациями: среди возбудителей в 48% случаев выделяются облигатные (Prevotella – 31%, Fusobacterium – 15%) и факультативные (Streptococcus spp. – 22%) анаэробы. У 52% пациентов встречаются аэробы: различные Streptococcus spp. – 21%, Haemophilus influenzae (гемофильная палочка) – 16%, Pseudomonas aeruginosa (синегнойная палочка) – 15%, Staphylococcus aureus (золотистый стафилококк) и Moraxella spp. (моракселла) – по 10%. Преобладание анаэробов при хроническом синусите можно объяснить изменениями, происходящими в пазухах: в первую очередь, ухудшением аэрации пазухи и снижением рН, что создает благоприятные условия для развития этих микроорганизмов. Грибковый синусит, вызываемый грибами Aspergillus, Phycomycetes (Mucor, Rhizopus), Alternaria, Candida является особой формой хронического синусита и встречается значительно реже бактериального.
Оптимальными препаратами, максимально воздействующими на основных бактериальных возбудителей обострения хронического синусита, являются амоксициллина/клавуланат и респираторные фторхинолоны (левофлоксацин, моксифлоксацин).
Амоксициллин/клавуланат обладает широким спектром антибактериального действия (грамположительные и грамотрицательные микроорганизмы, анаэробы, включая штаммы, продуциру-ющие b–лактамазу), действует бактерицидно. Механизм действия: блокирование синтеза пептидогликана оболочки микробной клетки (амоксициллин), ингибирование b–лактамазы (клавулановая кислота).
В связи с хорошей переносимостью амоксициллина/клавуланата, а также отсутствием тяжелых побочных эффектов препарат широко используется не только для лечения взрослых пациентов, но и в педиатрической практике.
Левофлоксацин (Элефлокс) является представителем нового поколения фторхинолонов. Преимуществом данной группы перед фторхинолонами первого поколения является их высокая активность в отношении грамположительных бактерий, прежде всего – пневмококков и стрептококков. Механизм антимикробного действия левофлоксацина связан с ингибированием ДНК–гиразы – основного фермента бактериальной клетки, ответственного за процесс нормального биосинтеза ДНК.
Левофлоксацин характеризуется широким антимикробным спектром (грамположительные и грамотрицательные аэробные бактерии и неклостридиальную анаэробную флору, атипичные микроорганизмы), благоприятными фармакокинетическими свойствами (высокая биодоступность, хорошее проникновение в ткани, длительный период полувыведения), позволяющим применять препарат 1 раз в сутки (по 500 мг), хорошей переносимостью и отсутствием серьезных нежелательных эффектов, отмеченных при применении других фторхинолонов (фототоксичность, гепатотоксичность, судороги, удлинение интервала QT), по сравнению с амоксициллином/клавуланатом левофлоксацин также характеризуется лучшей переносимостью (частота нежелательных реакций достоверно значительно ниже в группе левофлоксацина по сравнению с группой амоксициллина/клавуланата).
При выборе антибактериального препарата немаловажным фактором является доверие тем или иным производителям (особенно в случае выбора дженериков). В ЛОР–практике с успехом применяется левофлоксацин под торговым наименованием Элефлокс, который выпускается фармацевтической компанией Ranbaxy.*
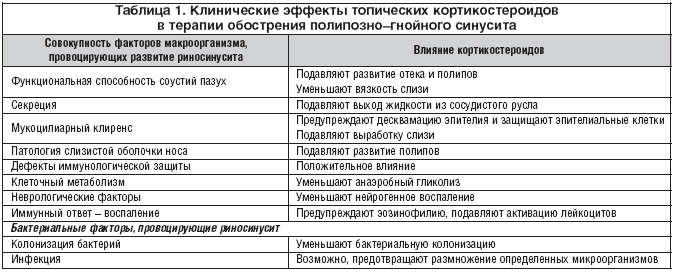
Вышеописанные антибактериальные препараты наиболее эффективны в комбинации с топическим кортикостероидом (мометазона фуроат в дозировке для взрослых 200 мкг/сутки) и деконгестантом. Включение в схему лечения топических кортикостероидов ускоряет клиническое улучшение, прежде всего за счет уменьшения отека, снятия назальной обструкции, восстановления аэрации и улучшения дренажной функции соустьев ОНП. Кроме того, при цитологическом исследовании мазков–отпечатков со слизистой оболочки полости носа в ходе многочисленных клинических исследований было зарегистрировано достоверное снижение числа нейтрофилов, базофилов и эозинофилов [3].
Вышеуказанные эффекты топических кортикостероидов в комбинации с респираторными фторхинолонами в терапии обострения полипозно–гнойного синусита наглядно иллюстрированы в таблице 1.
Основными антимикотическими препаратами при лечении грибковых синуситов являются флуконазол и амфотерицин В. Схема использования, дозировка данных препаратов определяются индивидуально, с учетом особенностей пациента и клинического течения заболевания.
Основой выбора метода хирургического лечения пациентов данной группы является функциональное состояние слизистой оболочки ОНП. Нами разработан алгоритм, основанный на объективных критериях, который поможет практикующему врачу в выборе хирургической тактики в каждом конкретном случае (табл. 2).
При обратимых изменениях слизистой оболочки ОНП показано функциональное эндоскопическое вмешательство с сохранением слизистой оболочки ОНП, при необратимых изменениях – полное удаление слизистой оболочки синуса в ходе радикального вмешательства.
Основной целью функциональной эндоскопической хирургии является атравматичное удаление полипов при помощи шейвера (микродебридера), реконструкция зоны остиомеатального комплекса и восстановление вентиляции и дренажа пораженных ОНП через естественные соустья.
При необратимых изменениях слизистой оболочки ОНП (по данным функциональных исследований), помимо выполнения эндоназального эндоскопического вмешательства с тщательным вскрытием клеток решетчатого лабиринта и необходимой коррекцией эндоназальных структур, показана радикальная операция на синусе с полным удалением слизистой оболочки, наложением искусственного соустья с нижним носовым ходом, обязательной тампонадой ОНП наливным латексным тампоном. Именно латексная тампонада позволяет сформировать и сохранить лейкоцитарно–некротический (фибриновый) слой, являющийся основой для полноценной эпителизации послеоперационной полости мерцательным эпителием [4].
Проведение антибактериальной терапии (респираторные фторхинолоны) в комбинации с топическим кортикостероидом во время активной фазы бактериального воспаления, выполнение адекватной хирургической санации очага инфекции в период ремиссии синусита – эффективные мероприятия профилактики рецидива полипозного процесса у пациентов данной группы.
Полипоз, развивающийся на фоне аспириновой триады (ассоциированный с атопической
бронхиальной астмой, атопией)
Данный вид полипозного процесса являетсся наиболее проблемным в отношении рецидивирования полипозного процесса. Все дело в том, что при аспириновой триаде полипозный процесс в полости носа и ОНП является одним из симптомов заболевания всего организма, связанного с нарушением метаболизма арахидоновой кислоты, иммунологическими изменениями (реагиновый тип аллергической реакции, связанный с выработкой специфических IgE). Хирургическое лечение пациентов с полипозным этмоидитом, ассоциированным с бронхиальной астмой, без соответствущей консервативной терапии в до– и послеоперационный период, неминуемо заканчивается рецидивом полипозного процесса. Более того, проведение хирургического вмешательства у данной категории больных без специальной предоперационной подготовки может спровоцировать некупируемый приступ бронхиальной астмы. Обязательным условием является проведение хирургического лечения вне обострения бронхиальной астмы и поллиноза. Общепринятая схема предоперационной подготовки следующая: 1) использования топических кортикостероидов эндоназально (мометазон, флутиказон) за 14–30 дней до хирургического лечения; 2) преднизолон 60–90 мг или дексаметазон 8–16 мг внутривенно капельно 1 раз в сутки за 3 дня до и 3 дня после операции.
Хирургическое лечение состоит в полипэтмоидотомии с тотальным вскрытием решетчатого лабиринта и полисинусотомии с использованием эндоскопической (микроскопической) техники.
Послеоперационное ведение пациентов с полипозным гаймороэтмоидитом подразумевает необходимость длительного использования топических кортикостероидов эндоназально в послеоперационном периоде. Цель применения данных препаратов заключается в профилактике возникновения рецидивов полипозного процесса. Топические кортикостероиды последнего поколения (мометазона фуроат) обладают минимальным системным действием, применяются в виде спрея по 2 дозы (200 мкг/сутки) в каждый носовой ход ежедневно в течение 6–12 месяцев, с началом использования через 7–10 дней после перенесенной операции. Затем совместно с аллергологом (пульмонологом) решается вопрос о курсовом применении препарата в течение длительного времени (1,5 месяца используется, затем на 1,5 месяца прекращение терапии и т.д.).
Подводя итог, хочется подчеркнуть значимость дифференцированного подхода в лечении пациентов с полипозным синуситом. Органичное сочетание хирургических и консервативных мероприятий, гибкий индивидуальный подход в каждой конкретной клинической ситуации являются залогом успешного лечения.
*Примечание редактора. Компания Ranbaxy является частью компании Daiichi Sankyo – разработчика молекулы левофлоксацина. Руководит Ranbaxy один из первооткрывателей левофлоксацина – г–н Тсутому Уне

Литература
1. Bachert C. et al. // ACI International. 1999. V. 11. P. 130.
2. Ponikau J.U. et al. // Mayo Clin. Proc. 1999. V. 74. P. 877.
3. Treatment of congestion in upper respiratory diseases / E. O. Meltser et al. // Int. J. Gen. Med. 2010. Vol. 3. P. 69–91.
4. Состояние верхнечелюстных пазух в отдаленном послеоперационном периоде при различных вариантах санирующей хирургии. // Вестник оториноларингологии / Москва, 2003, №3, с.4–9. (Крюков А.И., Сединкин А.А., Антонова Н.А. , М.Н. Шубин).
Крюков А.И., Туровский А.Б., Сединкин А.А.
РМЖ

 Опубликовано в категории:
Опубликовано в категории:  Метки:
Метки: